
近日,中心与东部战区总医院肾脏病中心合作, 运用奥根诊断AlloK seqTM [安康] 肾移植无创检测平台, 对50例疑似排斥患者进行了回顾性研究, 揭示了供体来源游离DNA(ddcfDNA)在中国肾移植患者中诊断抗体介导排斥反应的价值。相关成果发表于国际器官移植领域权威杂志《Transplant Immunology》。
在这项回顾观察性研究中,纳入了自2018年6月至2019年5月在东部战区总医院诊断为疑似排斥反应的肾移植受者50例,采用AlloK seqTM靶向捕获测序方法检测血浆中ddcfDNA的浓度。根据病理穿刺(是否ABMR) 和供体特异性抗体(DSA)的结果, 临床上将患者分为四组: ABMR+/DSA+、ABMR+/DSA-、ABMR-/DSA和ABMR-/DSA-。结果显示ABMR+组ddcfDNA浓度的中位数(1.66%,IQR 1.34-3.76%)显著高于ABMR-组(0.63%,IQR 0.43-0.74% ; p < 0.001)。 受试者工作特征曲线 (ROC) 分析其曲线下面积 (AUC) 为0.90(95%CI,0.86–0.95),当设定ddcfDNA阈值为0.96%时,检测敏感性为90.5%(95%CI,69.6–98.8%),特异性为96.6%(95%CI,82.2–100%),PPV为95%(95%CI,73.4–99.2%),NPV为93.3%(95%CI,78.9–98.1%)。准确性远高于DSA诊断ABMR (特异性为50%,敏感性为74.1%,PPV为41.7%,NPV为80%)。在DSA+组和DSA-组中ddcfDNA无显著性差异(p>0.05)。研究提示无论DSA阳性或阴性,只要ddcfDNA升高, 都有可能发生ABMR, ddcfDNA可以用来独立精准的诊断ABMR的发生。
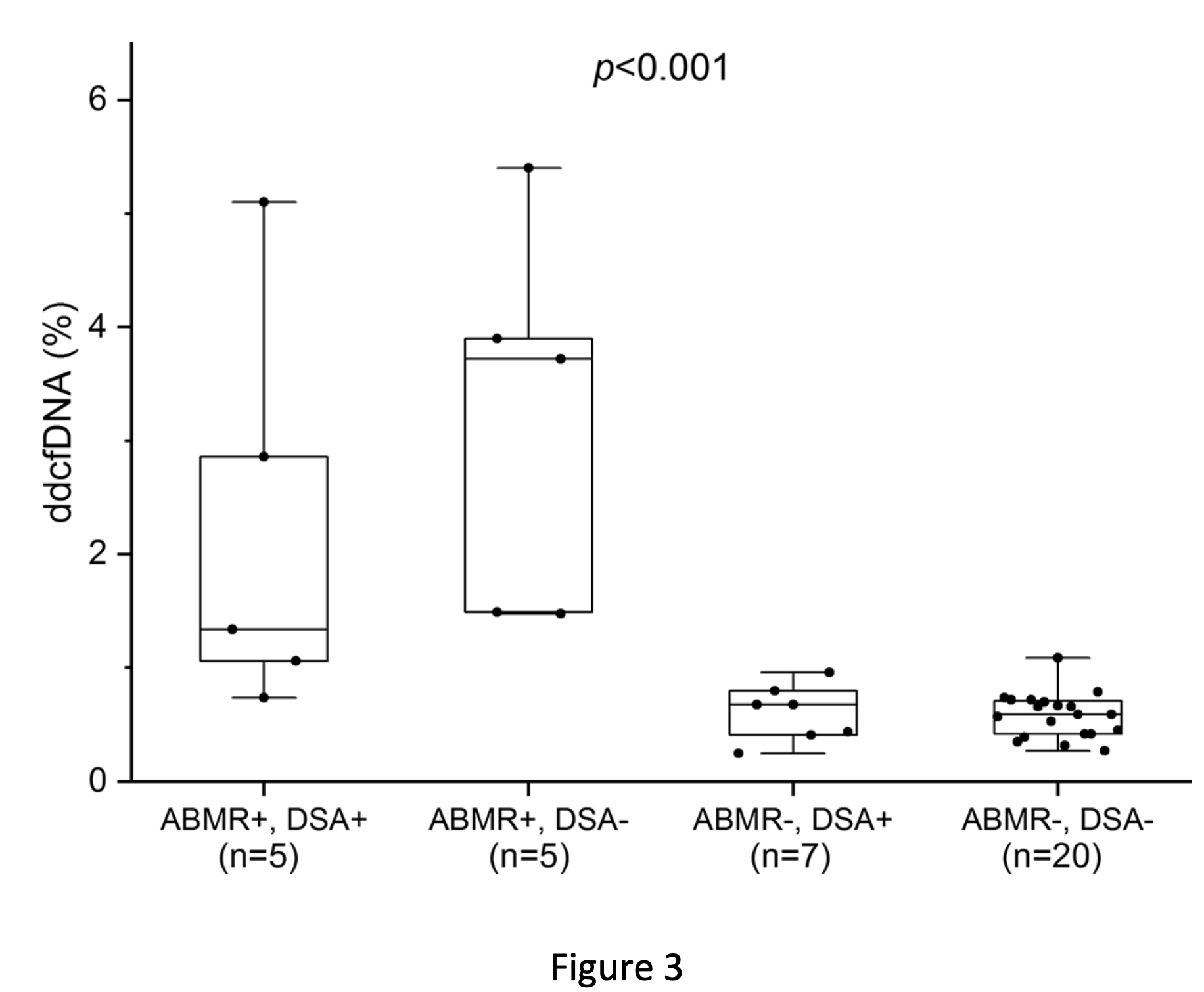
ddcfDNA是一种新型的器官移植无创诊断生物标志物,在肾移植上与传统标志物 (血清肌酐, 抗体等) 相比,具有较高的特异性和敏感性。自2018年临床应用以来, 目前在国外肾移植中心已常规开展, 累计检测患者数超过15万例。本研究中首次在中国人群中评估AlloK seqTM在抗体介导排斥反应中的价值, 为中国肾移植患者排斥反应的诊断提供了一个精准的无创方法。
推荐阅读:
中心合作单位奥根诊断荣获国家高新技术企业认定
中心合作单位成功研发一种新型尿液cfDNA常温保存管
中心合作单位早期肾移植供体来源游离DNA(ddcfDNA)检测技术论文被Nature 5月子刊引用